复旦大学徐建青团队研制可同时预防新冠和流感病毒的新型疫苗
时间:2022-03-03
近日,复旦大学生物医学研究院徐建青研究员团队通过融合新冠病毒受体结合域(RBD)与流感病毒H7N9血凝素(HA)保守区,设计了一种合成免疫原,并通过腺病毒载体(AdC68)表达,构建出一种可以同时对SARS-CoV-2和IAV提供双重保护的新型疫苗。研究成果近期以题为“A Single Vaccine Protects against SARS-CoV-2 and Influenza Virus in Mice”的论文在线发表于国际高水平杂志Journal of Virology。

面对严重的新冠病毒疫情,疫苗研发工作受到了极大关注。目前有近百种疫苗进入临床试验阶段,其中的几种已广泛接种于人群。然而,不断出现的可以逃避中和抗体的变异毒株和新冠病毒的季节性变化表明疫苗开发需要持续努力。在新冠病毒出现之前,A型流感病毒(IAV)是导致呼吸道疾病的主要病毒,对全球健康和经济构成严重威胁,1918年和2009年H1N1大流行以及最近的2013年H7N9疫情证明了这一点。因此本研究旨在开发一种能够同时对SARS-CoV-2和IAV提供双重保护的疫苗。
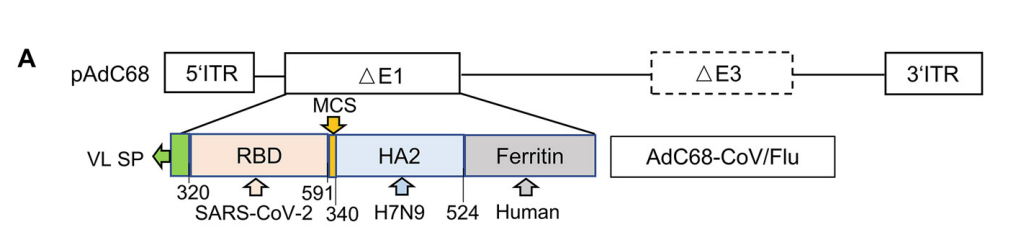
研究人员首先通过将新冠病毒RBD(320-591aa)和H7N9血凝素HA2(340-524aa)由编码9个氨基酸(VDELTSRGR)的多克隆位点链接,设计出了一种融合免疫原。此外将小鼠IgGk轻链作为ER信号肽连接到免疫原N端,将人铁蛋白构建到C端。该设计中铁蛋白附着在免疫原的C末端,可以促进HA2-RBD的多聚化,这是因为铁蛋白具有自组装成包含24个单体的纳米颗粒(NP)的天然能力,从而允许通过多价相互作用更有效地结合抗原特异性B细胞。最后实验人员选择黑猩猩腺病毒AdC68作为表达载体进行表达,并将此疫苗命名为AdC68-CoV/Flu。
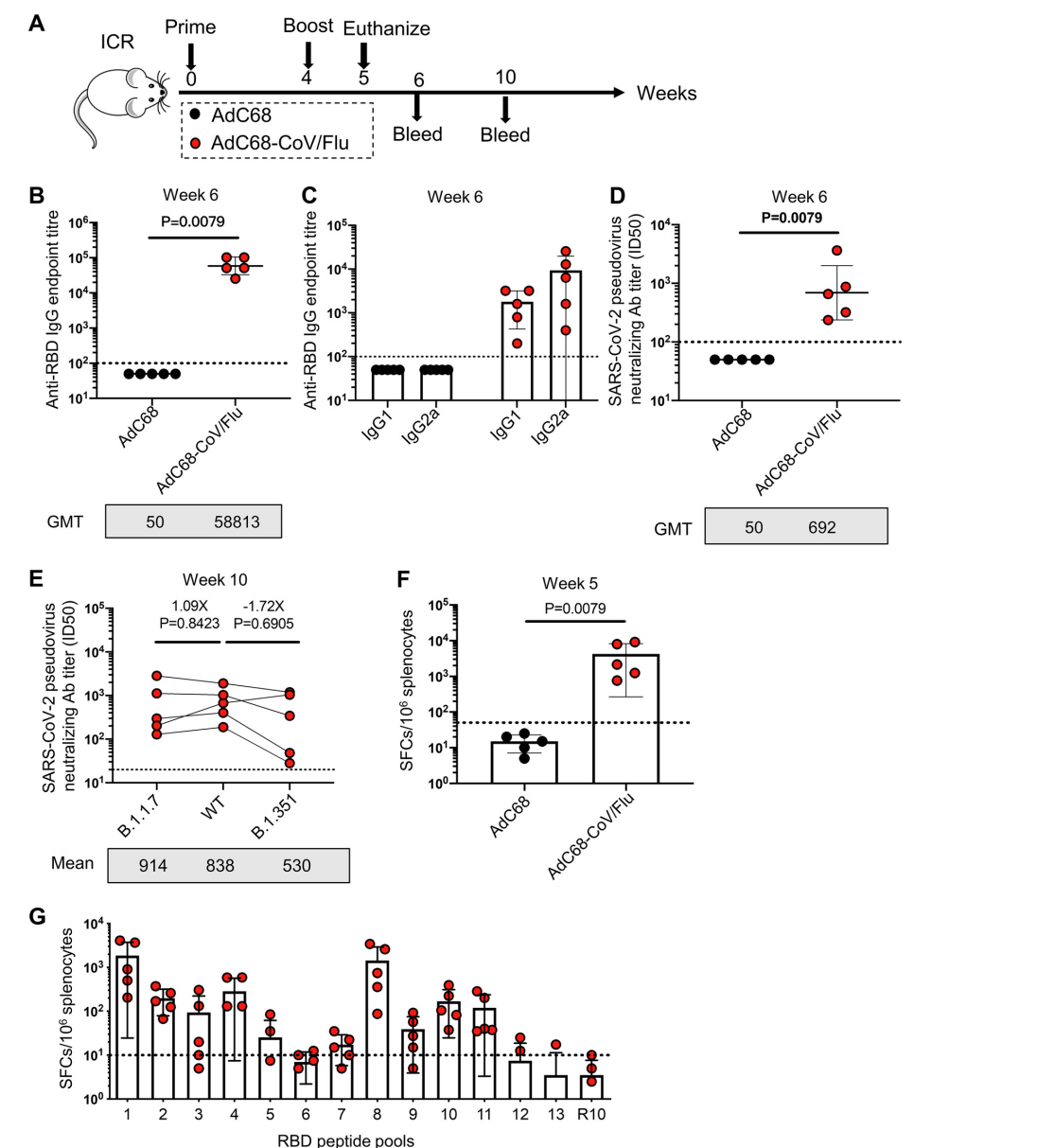
接下来,研究人员对AdC68-CoV/Flu在小鼠中的免疫原性进行了实验。结果表明AdC68-CoV/Flu在对抗新冠病毒及其变异株的有效抗体反应中具备良好潜力。此外,鉴于腺病毒在诱导针对插入免疫原的T细胞免疫反应方面的强大能力,研究人员评估了在免疫后第5周从免疫小鼠分离的脾细胞的RBD特异性T细胞反应情况,结果显示强烈的T细胞反应可能提供额外的机制来阻止变异株从中和抗体中逃逸。
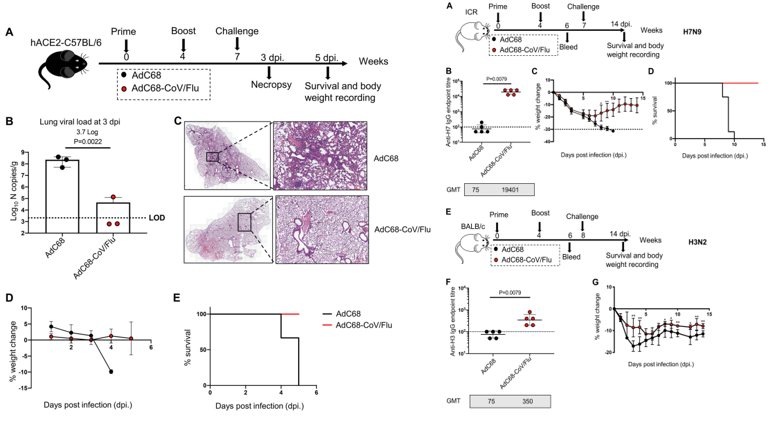
在随后的攻毒实验中,采取实验第三天小鼠肺部样本以进行病毒载量和组织病理学评估。通过RT-qPCR对病毒的转录物产物进行检测,结果表明与对照动物相比,接受AdC68-CoV/Flu的小鼠的病毒载量明显降低。肺组织HE染色进一步显示,疫苗可改善病毒感染诱导的病理学变化,最大限度地减少细支气管上皮破坏,并显著减少炎症浸润。此外,所有未接种AdC68-CoV/Flu组的hACE2转基因小鼠均在5天后死亡,且体重出现明显下降。而接种疫苗组的小鼠没有出现任何体重减轻的迹象,并且在观察期内全部存活。这表明AdC68-CoV/Flu在hACE2转基因小鼠中对预防新冠病毒感染中非常有效。进一步的研究表明AdC68-CoV/Flu在控制流感病毒时同样发挥作用,能够针对H7N9和H3N2两种病毒提供交叉保护。
该研究得到国家自然科学基金(81761128007, 81430030, 82071788)、国家“十三五”重大传染病防治规划基金(2017ZX10202102)、上海市浦江项目(19PJ1409100)、上海市科委(18DZ2293000)等项目的资助。
全文链接:https://doi.org/10.1128/jvi.01578-21
转自 病毒学界:原文阅读

